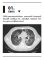
Hematológiai betegek CMV-fertőzései
Hematológiai daganatos megbetegedés esetén és őssejt-transzplantációt követően a CMV-reaktiváció fokozza a szövődmények előfordulását, és növeli a halálozás kockázatát. A közlemény összefoglalót nyújt a kockázati tényezőkről, bemutatja a megjelenési formákat és az ellátási stratégiákat.
A teljes cikket csak regisztrált felhasználóink olvashatják. Kérjük jelentkezzen be az oldalra vagy regisztráljon!
A kulcsos tartalmak megtekintéséhez orvosi regisztráció (pecsétszám) szükséges, amely ingyenes és csak 2 percet vesz igénybe.
a szerző cikkei