Addison-kór: korai felismerés és a kezelés alapelvei
A primer mellékvesekéreg-elégtelenség okai közül az autoimmun mellékvesekéreg-gyulladás a leggyakoribb. A következmény a glükokortikoidok, a mineralokortikoidok és a mellékvesében képződő androgének hiánya. Fontos, hogy gondoljunk a betegség lehetőségére és felismerjük az életveszélyes Addison-krízist, figyeljünk az azt megelőző enyhe tünetekre is. Ha felmerül a gyanú, cosyntropin stimulációs teszttel igazolhatjuk a diagnózist. A primer mellékvesekéreg-elégtelenség kezelése a glükokortikoidok és a mineralokortikoidok pótlását jelenti. Az autoimmun mellékvesekéreg-gyulladáshoz sokszor egyéb autoimmun gyulladás is társul.
Több mint 150 évvel ezelőtt Thomas Addison azonosított egy anémiás betegcsoportot, akiknél később a boncolás kóros mellékvese-elváltozást talált. Az Addison által leírt állapotot ma primer mellékvesekéreg-elégtelenségnek nevezzük. Az Egyesült Államokban a primer mellékvesekéreg-elégtelenség vagy Addison-kór leggyakoribb oka az autoimmun mellékvesekéreg-gyulladás. A kevésbé gyakori okok közé tartozik a gyulladás, a hemorrágia, az áttétes karcinóma, a gyógyszermellékhatás és az adreno-leukodisztrófia. Az autoimmun mellékvesekéreg-gyulladás során a mellékvesekéreg elpusztul, ezért megszűnik a glükokortikoidok, mineralokortikoidok és adrenális androgének termelése. Az Addison-kór jelentkezhet az autoimmun poliglanduláris szindrómák (1-es, illetve 2-es típus) részeként, de önálló megbetegedés formájában is. (1) A jelen tanulmány az önállóan jelentkező Addison-kór diagnózisára és terápiájára fókuszál, ezen belül az autoimmun mellékvesekéreg-gyulladás kórélettanára és kezelésére helyezi a hangsúlyt.
Patogenezis
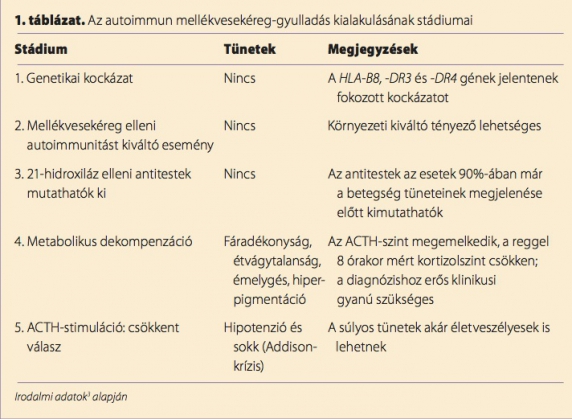
Az autoimmun mellékvesekéreg-gyulladás kórfejlődése különböző stádiumokra osztható (2,3) (1. táblázat). A betegség kialakulásakor néhány éven belül megszűnik a mellékvesekéreg működése. Az első három stádiumban a HLA- (humán leukocita antigén) gének genetikai kockázatot jelenthetnek; a mellékvesekéreg elleni autoimmun védekezést egyelőre ismeretlen esemény indítja be. A 21-hidroxiláz elleni antitestek megjelenése előrejelzi a betegség létrejöttét. Az antitestek képződése évekkel vagy akár évtizedekkel megelőzheti a tünetek kialakulását, és az antitestek az új keletű esetek több mint 90%-ában kimutathatók. (2,4–7) A negyedik stádiumban nyilvánvalóvá válik a mellékvesekéreg-elégtelenség. Az egyik első metabolikus rendellenesség a plazma reninszintjének megemelkedése, amit más rendellenességek egymás utáni kifejlődése követ, köztük az ACTH-stimulációs tesztre adott válasz csökkenése az ötödik stádiumban. Ha a mellékvesekéreg-elégtelenség tünetei jelen vannak, de diagnosztizálásuk elmarad, Addison-krízis alakulhat ki.
 Klinikai diagnózis
Klinikai diagnózis
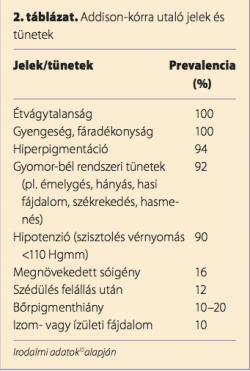
Mivel az USA-ban és Nyugat-Európában az Addison-kór becsült prevalenciája 1/20 000 fő, fontos, hogy gondoljunk a betegség lehetőségére, és elkerüljük az életveszélyes Addison-krízis félrediagnosztizálását. (8) A betegségre utaló jelek és tünetek enyhék, nem specifikusak is lehetnek. A betegek kimerültséget, gyengeséget, testsúlyvesztést és gyomor-bél rendszeri működészavarokat panaszolhatnak (9) (2. táblázat). A tünetek fokozatosan alakulnak ki, és évek alatt rosszabbodnak, ami nehézzé teszi a korai diagnózist. (10) A tünetek a kortizol-, a mineralokortikoid- és az adrenális androgén hiány aktuális mértékével korrelálnak. Az Addison-kórt általában jelentős stressz vagy betegség kapcsán diagnosztizálják, amikor a kortizol- és mineralokortikoidhiány nyilvánvalóvá válik: sokk, hipotenzió és folyadékvesztés (adrenális vagy Addison-krízis) jelentkezik. (11) A kortizol- és aldoszteronhiány hozzájárul a hipotenzió, az ortosztázis és a sokk kialakulásához. Primer mellékvesekéreg-elégtelenség esetén nagyobb az Addison-krízis kialakulásának esélye, mint szekunder mellékvesekéreg-elégtelenségben.
Az Addison-kórra legjellemzőbb fizikális tünet a hiperpigmentáció. Ennek oka az agyalapi mirigy elülső részének folyamatos kortikotrop aktivitása, konkrétabban a hipofízis által termelt ACTH és a keratinociták melanokortin-1-receptorai közti keresztreaktivitás. A hiperpigmentáció általában generalizáltan jelentkezik az egész testen, és különösen kifejezett a tenyér barázdáiban, valamint a szájnyálkahártyában, az ajakhatáron, a mellbimbók és bőrhegek körül. Szekunder mellékvesekéreg-elégtelenségben nincs hiperpigmentáció, mivel ilyenkor nem fokozódik az ACTH-termelés.
Diagnózis
Metabolikus tesztek
A laboratóriumi vizsgálatok célja az alacsony kortizolszint kimutatása és annak megállapítása, hogy primer vagy szekunder mellékvesekéreg-elégtelenségről van-e szó. A diagnosztikus folyamatot az 1. ábra szemlélteti. A reggel 8 órakor mért alacsony szérumkortizol (11 pmol/l) értékek kortizolhiányra utalnak. (7) A mellékvesekéreg-elégtelenség diagnosztizálásának első vonalbeli eszköze a cosyntropin stimulációs teszt. A szérumkortizol-, plazma-ACTH-, plazmaaldoszteron- és plazmareninszinteket 250 μg ACTH beadása előtt mérik, majd a kortizolmérést megismétlik 30 és 60 perccel az ACTH intravénás beadása után. Normális válasz esetén a kortizol maximális szérumszintje magasabb 497–552 nmol/l-nél; az ennél alacsonyabb szintű, illetve a hiányzó válasz mellékvesekéreg-elégtelenséget jelent. (14,15)
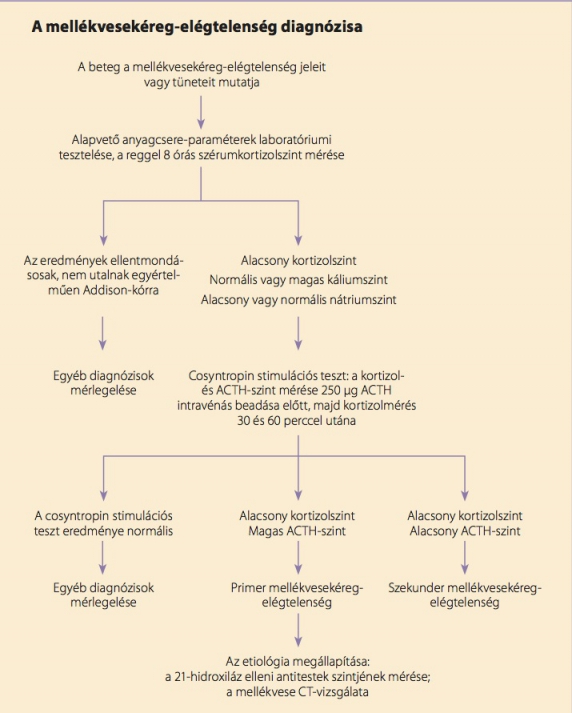
1. ábra. A mellékvesekéreg-elégtelenség diagnosztizálásának algoritmusa
Immunológiai tesztek
A 21-hidroxiláz elleni antitestek mérése segít az Addison-kór okának megállapításában. A 21-hidroxiláz enzim szükséges ahhoz, hogy a mellékvesekéreg kortizolt szintetizáljon, és az ellene képződött antitestek jelenléte autoimmun mellékvesekéreg-gyulladásra utal, ami így már a tünetek megjelenése előtt kimutatható.
Képalkotó eljárások
A radiológiai eljárások hasznosak lehetnek az Addison-kór okának megállapításában, ám a módszer kevéssé specifikus autoimmun gyulladásban szenvedő betegek esetében. Fontos, hogy a mellékvesekéreg-elégtelenség biokémiai diagnózisa a radiológiai képalkotás előtt megtörténjen. A CT autoimmun gyulladásban kisméretű mellékveséket mutat. Más okból bekövetkező Addison-kórban a CT vérzést, tuberkulózishoz kapcsolódó meszesedést vagy tumoros szövetet mutathat ki a mellékvesékben. Mindamellett a CT nem feltétlenül szükséges a mellékvesekéreg-elégtelenség diagnosztizálásához.
Kezelés
Hormonterápia
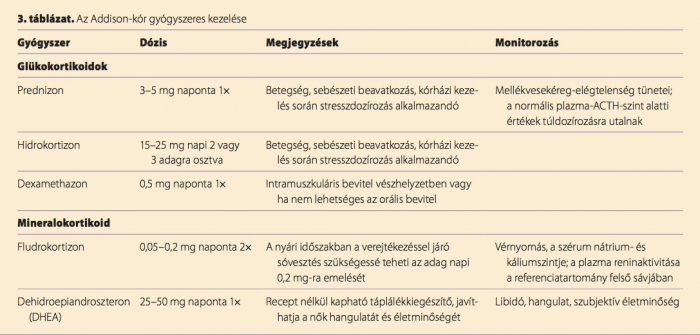
Az Addison-kór kezelése a glükokortikoid és mineralokortikoid hormonok élethosszig tartó pótlásából áll (3. táblázat). (16) Jelenleg nem áll rendelkezésünkre olyan oki terápia, amellyel a mellékvesekéreg autoimmun pusztulását meg lehetne állítani. A glükokortikoidpótlás általában orális prednizon vagy hidrokortizon adását jelenti. (17) A prednizont naponta egyszer kell szedni, a hidrokortizont naponta kétszer vagy háromszor. (18–20) A mineralokortikoidokat fludrokortizonnal pótolhatjuk; a szert olyan dózisban kell adni, hogy a plazma reninszintje a referenciatartomány felső határánál legyen. (21,22)
Az Addison-kórban szenvedő férfiak nem szorulnak androgénpótlásra, mivel a herék képesek megfelelő mennyiségű tesztoszteront termelni, a nők esetében azonban hasznos az androgénpótlás, mivel a női androgéntermelés fő helye a mellékvese. Tíz véletlen besorolásos, placebokontrollos klinikai vizsgálat metaanalízise szerint mellékvesekéreg-elégtelenségben szenvedő nők egészséggel összefüggő életminősége és depressziója kismértékben javult dehidroepiandroszteron (DHEA) adagolása következtében. (23)
Glükokortikoidok adása stresszállapotokban
A betegeket tájékoztatni kell arról, hogy betegségek kapcsán és műtéti beavatkozások előtt a glükokortikoidot emelt dózisban kell alkalmazniuk, mivel a mellékvese pusztulása miatt szervezetük nem ad megfelelő fiziológiás választ a stresszhatásokra. (24) Sok ajánlás készült szakemberek számára azzal kapcsolatban, hogy stressz idején milyen dózisban érdemes adni a szteroidokat; az ajánlások igyekeznek figyelembe venni a stressz mértékét. Az irodalomban nem található olyan klinikai vizsgálat, amely a különböző megközelítések hatékonyságát hasonlítaná össze. E sorok írói saját klinikai praxisukban olyan stresszdozírozási stratégiához folyamodnak, amelyet a betegek ambuláns beavatkozások (pl. kolonoszkópia, endoszkópia) és invazív fogorvosi eljárások (pl. gyökércsatorna-kezelés) alkalmával könnyen tudnak használni. Ezt a glükokortikoidok stresszdozírozása háromszor hármas szabályának nevezhetjük: a beavatkozás napján és még 2 napig a fenntartó glükokortikoiddózis háromszorosát kell használni.
Kisebb megbetegedések, pl. influenza vagy vírusos gasztroenteritisz esetén a betegség fennállásának ideje alatt a beteg szedjen háromszoros dózisú szteroidot, majd a tünetek megszűnése után térjen vissza a szokásos dozírozáshoz. Fontos, hogy arra az esetre, ha az orális bevitel nem megoldható (pl. hányinger, hányás miatt), a betegnek injektálható glükokortikoid is rendelkezésére álljon (im. dexamethazon). A mineralokortikoidpótlás általában nincs összefüggésben a betegségekkel vagy az orvosi beavatkozásokkal, de a nyári hónapokban, a jelentős mértékű izzadás és sóvesztés miatt, szükség lehet dóziskorrekcióra.
A kezeléssel kapcsolatos figyelmeztetések
Nem diagnosztizált Addison-kórban a pajzsmirigyhormon-terápia Addison-krízishez vezethet, mivel a pajzsmirigyhormon fokozza a kortizol lebontását a májban. Ezenkívül újonnan diagnosztizált Addison-kórban reverzibilisen megemelkedhet a TSH-szint, mivel a glükokortikoidok gátolják a pajzsmirigyhormon szekrécióját. (25,26) A glükokortikoidpótlás eredményeképpen a TSH-szint 30 mE/l alatti értéken normalizálódhat. Egyes típusú cukorbetegségben az Addison-kór kezdeti tünete lehet a látszólag ok nélkül kialakuló hipoglikémia és a csökkenő inzulinigény. (27)
Az Addison-kór hosszú távú kezelése
Az Addison-kórban szenvedő betegeket endokrinológussal együttműködve kell kezelni, és a megfelelő hormonterápia biztosítása érdekében fontos a betegek rendszeres ellenőrzése (3. táblázat). A glükokortikoid dózisát a legalacsonyabb, még tolerálható szintre kell kititrálni, hogy megszüntessük a tüneteket, de minimalizáljuk a mellékhatásokat. Elengedhetetlen, hogy a betegeknek megtanítsuk, hogyan kell a glükokortikoidokat dozírozni stressz esetén. A betegek rendelkezzenek injektálható glükokortikoiddal, és hordjanak maguknál az állapotukra figyelmeztető egészségügyi igazolványt.
Az autoimmun mellékvesekéreg-gyulladás miatt Addison-kórban szenvedők mintegy felénél életük során más autoimmun megbetegedés is kialakul, ezért gondozásuk során mindig figyelni kell további autoimmun megbetegedések esetleges felbukkanására. (28,29) A 4. táblázat bemutatja, hogy mely autoimmun kórképek fordulnak elő az Addison-kórral együtt, ezek mennyire elterjedtek, és milyen metabolikus tesztekkel milyen autoantitesteket kell keresni azoknál az Addison-kóros betegeknél, akik e betegségek valamelyikének kezdeti tüneteit mutatják. (8,28–34) Fontos szem előtt tartani, hogy az Addison-kóros nőbetegek 10%-a az autoimmun megbetegedés miatt korai petefészek-kimerülésben vagy primer petefészek-elégtelenségben is szenved, reproduktív életéveik során is jelentkeznek náluk az ösztrogénhiány tünetei (pl. amenorrea, hőhullámok, fáradtság, koncentrációzavar). (34) Javasoljuk számukra ennek kivizsgálását és a családalapítás alternatív lehetőségeivel kapcsolatos tanácsadáson való részvételt. (35)

Orvosok és betegek számára egyaránt hasznos információval szolgálnak a National Adrenal Diseases Foundation, valamint az Addison-kórosok önsegítő csoportja által működtetett honlapok: http://www.nadf. us és http://www.addisons.org.uk.

Az adatok forrásai. A szerzők a PubMed és a Cochrane adatbázisokban kerestek rá a témához kapcsolódó cikkekre, valamint használták az American Family Physician szerkesztőitől kapott Essential Evidence Plus összefoglalót. A keresési kifejezések a következők voltak: Addison disease, autoimmune primary adrenal insufficiency, cosyntropin stimulation testing, glucocorticoid treatment, mineralocorticoid treatment, DHEA treatment, the immunology of Addison disease. Az elmúlt 5 évben publikált, angol nyelvű, absztrakttal rendelkező cikkek álltak a keresés fókuszában; az Addison-kór jelei, tünetei és diagnózisa kapcsán 5 évesnél régebbi cikkeket is idéztünk, ahol azt jónak láttuk. Keresési időpontok: 2011. december és 2013. október.
Nyilatkozat. A szerzők nem jeleztek érdekütközést.
ADDISON DISEASE: EARLY DETECTION AND TREATMENT PRINCIPLES • VOL 89 / NO 7 / APRIL 1, 2014 / AMERICAN FAMILY PHYSICIAN
Levelezési cím: This e-mail address is being protected from spambots. You need JavaScript enabled to view it.
Irodalom:
1. Michels AW, Eisenbarth GS. Immunologic endocrine disorders. J Allergy Clin Immunol 2010;125(Suppl 2):S226–S237
2. Betterle C, Dal Pra C, Mantero F, Zanchetta R. Autoimmune adrenal insufficiency and autoimmune polyendocrine syndromes: autoantibodies, autoantigens, and their applicability in diagnosis and disease prediction. Endocr Rev 2002;23(3):327–364. [Hibaigazítás: Endocr Rev 2002;23(4):579]
3. Eisenbarth GS, Gottlieb PA. Autoimmune polyendocrine syndromes. N Engl J Med 2004;350(20):2068–2079
4. Betterle C, Volpato M, Rees Smith B, et al. II. Adrenal cortex and steroid 21-hydroxylase autoantibodies in children with organ-specific autoimmune diseases: markers of high progression to clinical Addison’s disease. J Clin Endocrinol Metab 1997;82(3):939–942
5. Betterle C, Volpato M, Rees Smith B, et al. I. Adrenal cortex and steroid 21-hydroxylase autoantibodies in adult patients with organ-specific autoimmune diseases: markers of low progression to clinical Addison’s disease. J Clin Endocrinol Metab 1997;82(3):932–938
6. Coco G, Dal Pra C, Presotto F, et al. Estimated risk for developing autoimmune Addison’s disease in patients with adrenal cortex autoantibodies. J Clin Endocrinol Metab 2006;91(5):1637– 1645
7. Baker PR, Nanduri P, Gottlieb PA, et al. Predicting the onset of Addison’s disease: ACTH, renin, cortisol, and 21-hydroxylase autoantibodies. Clin Endocrinol (Oxf) 2012;76(5):617–624
8. Erichsen MM, Løvås K, Skinningsrud B, et al. Clinical, immunological, and genetic features of autoimmune primary adrenal insufficiency: observations from a Norwegian registry. J Clin Endocrinol Metab 2009;94(12):4882–4890
9. Burke CW. Adrenocortical insufficiency. Clin Endocrinol Metab 1985;14(4):947–976
10. Bleicken B, Hahner S, Ventz M, Quinkler M. Delayed diagnosis of adrenal insufficiency is common: a cross-sectional study in 216 patients. Am J Med Sci 2010;339(6):525–531
11. Bouachour G, Tirot P, Varache N, Gouello JP, Harry P, Alquier P. Hemodynamic changes in acute adrenal insufficiency. Intensive Care Med 1994;20(2):138–141
12. Schmidt IL, Lahner H, Mann K, Petersenn S. Diagnosis of adrenal insufficiency: evaluation of the corticotropin-releasing hormone test and basal serum cortisol in comparison to the insulin tolerance test in patients with hypothalamic-pituitary-adrenal disease. J Clin Endocrinol Metab 2003;88(9):4193–4198
13. Betterle C, Scalici C, Presotto F, et al. The natural history of adrenal function in autoimmune patients with adrenal autoantibodies. J Endocrinol 1988;117(3):467–475
14. Dickstein G, Shechner C, Nicholson WE, et al. Adrenocorticotropin stimulation test: effects of basal cortisol level, time of day, and suggested new sensitive low dose test. J Clin Endocrinol Metab 1991;72(4):773–778
15. May ME, Carey RM. Rapid adrenocorticotropic hormone test in practice. Retrospective review. Am J Med 1985;79(6):679–684
16. Arlt W, Allolio B. Adrenal insufficiency. Lancet 2003;361(9372):1881–1893
17. Crown A, Lightman S. Why is the management of glucocorticoid deficiency still controversial: a review of the literature. Clin Endocrinol (Oxf) 2005;63(5):483–492
18. Bleicken B, Hahner S, Loeffler M, et al. Influence of hydrocortisone dosage scheme on health-related quality of life in patients with adrenal insufficiency. Clin Endocrinol (Oxf) 2010;72(3):297–304
19. Debono M, Ross RJ, Newell-Price J. Inadequacies of glucocorticoid replacement and improvements by physiological circadian therapy. Eur J Endocrinol 2009;160(5):719–729
20. Quinkler M, Hahner S. What is the best long-term management strategy for patients with primary adrenal insufficiency? Clin Endocrinol (Oxf) 2012;76(1):21–25
21. Smith SJ, MacGregor GA, Markandu ND, et al. Evidence that patients with Addison’s disease are undertreated with fludrocortisone. Lancet 1984;1(8367):11–14
22. Oelkers W, Diederich S, Bähr V. Diagnosis and therapy surveillance in Addison’s disease: rapid adrenocorticotropin (ACTH) test and measurement of plasma ACTH, renin activity, and aldosterone. J Clin Endocrinol Metab 1992;75(1):259–264
23. Alkatib AA, Cosma M, Elamin MB, et al. A systematic review and metaanalysis of randomized placebo-controlled trials of DHEA treatment effects on quality of life in women with adrenal insufficiency. J Clin Endocrinol Metab 2009;94(10):3676–3681
24. Oelkers W, Diederich S, Bähr V. Therapeutic strategies in adrenal insufficiency. Ann Endocrinol (Paris) 2001;62(2):212–216
25. Kannan CR. Diseases of the adrenal cortex. Dis Mon 1988;34(10):601–674
26. Samuels MH. Effects of variations in physiological cortisol levels on thyrotropin secretion in subjects with adrenal insufficiency: a clinical research center study. J Clin Endocrinol Metab 2000;85(4):1388–1393
27. Armstrong L, Bell PM. Addison’s disease presenting as reduced insulin requirement in insulin dependent diabetes. BMJ 1996;312(7046):1601–1602
28. Zelissen PM, Bast EJ, Croughs RJ. Associated autoimmunity in Addison’s disease. J Autoimmun 1995;8(1):121–130
29. Kasperlik-Zaluska AA, Migdalska B, Czarnocka B, Drac-Kaniewska J, Niegowska E, Czech W. Association of Addison’s disease with autoimmune disorders – a long-term observation of 180 patients. Postgrad Med J 1991;67(793):984–987
30. Blizzard RM, Chee D, Davis W. The incidence of adrenal and other antibodies in the sera of patients with idiopathic adrenal insufficiency (Addison’s disease). Clin Exp Immunol 1967;2(1):19–30
31. McHardy-Young S, Lessof MH, Maisey MN. Serum TSH and thyroid antibody studies in Addison’s disease. Clin Endocrinol (Oxf) 1972;1(1):45–56
32. Nerup J. Addison’s disease – clinical studies. A report of 108 cases. Acta Endocrinol (Copenh) 1974;76(1):127–141
33. O’Leary C, Walsh CH, Wieneke P, et al. Coeliac disease and autoimmune Addison’s disease: a clinical pitfall. QJM 2002;95(2):79–82
34. Husebye ES, Løvås K. Immunology of Addison’s disease and premature ovarian failure. Endocrinol Metab Clin North Am 2009;38(2): 389–405
35. Baker V. Life plans and family-building options for women with primary ovarian insufficiency. Semin Reprod Med 2011;29(4):362–372
Kommentár
Addison-kór: korai felismerés és a kezelés alapelvei
 Dr. Igaz Péter
Dr. Igaz Péter
Az MTA doktora. Egyetemi docens, Semmelweis Egyetem, II. Belgyógyászati Klinika, Budapest
A szerzők az Addison-kór gyakorlati szempontjait jól kiemelő összefoglaló cikket állítottak össze. Az Addison-kór ritka betegség, felismerése azonban több szempontból fontos. Egyrészt hatékonyan kezelhető, és a gyógyszeres kezeléssel a betegség jól karbantartható. Másrészt viszont a betegség fel nem ismerése súlyos következményekre vezethet (pl. Addison-kór okozta pszeudoperitonitisz műtéti beavatkozás esetén), illetve a szubsztitúciós kezelési dózisok akut helyzetekben történő megemelésének elmulasztása is végzetes lehet.
A hétköznapi klinikai gyakorlatban Addison-kór gyanúját kelti elsősorban a hiperpigmentáció, különösen a gingiván és a tenyérredőkben, valamint a normális vesefunkció mellett észlelt hiperkalémia. Ezek meglétekor különösen óvatosan kell eljárni hasi panaszok észlelése esetén, mivel Addison-krízis akut hasra emlékeztető klinikai képet okozhat, ugyanakkor az ilyen esetben végzett műtéti beavatkozás fatális kimenetelű lehet. Jellemző az Addison-kóros betegekre a gyengeség, szédülés, hipotónia, hányinger, hányás. Az ortosztatikus hipotónia kimutatása (Schellong-teszt) könnyen elvégezhető vizsgálat, és Addison-kórban gyakran pozitív.
Kóroktan, diagnosztika
Amint a szerzők is tárgyalják, a napjainkban előforduló Addison-kór döntően autoimmun adrenalitisz következménye. Ennek kialakulása lassú folyamat, ami klinikai tünetet akkor okoz, amikor a mellékvesekéreg lényegében már jelentősen károsodott. Az autoimmun adrenalitisz az esetek jelentékeny részében nem önállóan, hanem más szervspecifikus autoimmun betegségekkel társultan jelentkezik. Leggyakrabban az autoimmun poliendokrin szindróma 2-es típusa (APS-2) fordul elő, amelyben az Addison-kór mellett autoimmun pajzsmirigybetegségek, leginkább hipotireózis, 1-es típusú diabetes mellitus, valamint egyéb eltérések (pl. anaemia perniciosa, vitiligó, autoimmun hepatitisz) fordulnak elő. Már az 1920-as évek táján leírta Schmidt az Addison-kór és a hipotireózis társulását (Schmidt-szindróma), ami az APS-2 egyik formája. A Carpenter-szindróma Addison-kór, hipotireózis és diabetes mellitus társulását jelenti. Az Addison-kórhoz társuló manifeszt társbetegségekhez képest még gyakoribbak a látens kórképek, amelyekre az antitestek pozitivitása hívja fel a figyelmet (pl. Hashimoto-tireoiditiszre utaló anti-TPO-pozitivitás). Az autoszomális recesszív öröklődésű 1-es típusú autoimmun poliendokrin szindróma (APS-1) nagyon ritka kórkép, és döntően gyermekgyógyászati jelentőségű, bár napjainkban egyre több érintett éri meg a felnőttkort.
A II. világháború előtt az Addison-kór eseteinek döntő részéért a tuberkulózis volt felelős, ez azonban ma már a betegség ritka okai közé tartozik. A mellékvese áttétei előrehaladott rosszindulatú daganatos betegségekben (különösen tüdőrák esetén) előfordulnak, és kétoldali mellékveseáttétek kialakulása esetén Addison-kór léphet fel. A mellékvese kétoldali bevérzése szintén fontos oka lehet az Addison-kórnak, ez leginkább akutan fordul elő, jellemzően Neisseria meningitidis okozta szepszis esetén (Waterhouse–Friderichsen-szindróma).
Fontos megjegyezni, hogy Addison-kórról a mellékvesekéreg primer elégtelensége esetén beszélünk. A primer mellékvesekéreg-elégtelenséghez képest gyakoribb az agyalapi mirigy betegsége, az adrenokortikotropin (ACTH) hiánya következtében kialakuló szekunder mellékvesekéreg-elégtelenség (szekunder hipadrénia), amiben más hipofízishormonok hiánya is gyakori. Szemben a primer mellékvesekéreg-elégtelenséggel, szekunder hipadréniára a hiperkalémia kevéssé jellemző.
Az Addison-kór laboratóriumi diagnózisát az alacsony szérumkortizol mellett észlelt magas ACTH-szint képezi. Amennyiben az ACTH-meghatározás nem érhető el, az ACTH C-terminális 24 aminosavából készült peptid (tetracosactid) adásával végzett teszt alkalmazható. Addison-kórban alacsony az aldoszteronszint és magas a reninaktivitás. A laboratóriumi rutinvizsgálatok leletei között hiperkalémia és hiponatrémia mellett előfordulhat hiperkalcémia, valamint magas eozinofilszám is. (Történeti érdekesség, hogy a kortizol mérésének bevezetése előtt a hiperkortizolizmus diagnózisában felhasználták az eozinofil sejtszám jelentős csökkenését, az Addison-kóréban pedig az eozinofíliát.)
Terápia
Az Addison-kór kezelésében elsődleges a glükokortikoid- és mineralokortikoid-szubsztitúció. A hazai gyakorlatban glükokortikoidként elsősorban hidrokortizont alkalmazunk, amelynek napi dózisa 15–25 mg, és napi két-három részletben célszerű adni, a legnagyobb adagot reggel. A hidrokortizon mellett egyes betegek igénylik hosszabb hatástartamú glükokortikoid adását is, mivel reggelre elsősorban hányingerrel, szédüléssel jellemzett relatív hipadrénia alakulhat ki, amit prednizolon vagy dexamethazon esti bevételével kivédhetünk. Intenzív kutatások folynak a kortizol napszaki ritmusát jobban követő készítmények kifejlesztésére, amivel a betegek együttműködése is javítható lenne. Amennyiben a hidrokortizon nem érhető el (az utóbbi időben előfordult, hogy a hazai gyógyszertári forgalomban a hidrokortizon átmeneti hiánya jelentkezett), a szubszitúcióra naponta egyszer 4 mg metilprednizolon vagy 5 mg prednizolon is megfelelő. Mineralokortikoid-szubsztitúcióra fludrokortizont alkalmazunk napi kétszeri adagban (átlagosan napi 2×0,025–2×0,05 mg dózisban). Addison-kóros nőknek külföldön gyakran rendelnek dehidro-epiandroszteront (DHEA), általában napi 50 mg-os adagban, ami kedvezően befolyásolja a közérzetet, a libidót, az erőnlétet. Hazánkban a DHEA alkalmazása még nem terjedt el.
Az Addison-kór kezelésében az egyik legfontosabb gyakorlati probléma, hogy a glükokortikoid szubsztitúciós dózisát akut helyzetekben emelni kell. Műtéti beavatkozások, fertőzés, trauma esetén a betegnek több glükokortikoidra van szüksége. Az emelés mértékét a beavatkozás, illetve az állapotromlás mértéke szabja meg. Helyi érzéstelenítésben végzett beavatkozás esetén a napi dózis két-háromszorosának bevétele elegendő, ugyanakkor nagy hasi műtét esetén napi 3–4×100 mg infúziós hidrokortizon adása indokolt, amit a beavatkozás után fokozatosan kell leépíteni.
Mivel a hidrokortizon az aldoszteron receptorához is kötődik, nagy dózisú hidrokortizon adása esetén aldoszteront külön már nem kell adnunk. Nagyon fontos a betegeket körültekintően tájékoztatni arról, hogy nagyfokú gyengeség, szédülés, hányinger, rossz közérzet, láz esetén maguk kétszerezzék vagy háromszorozzák meg a hidrokortizon adagját. Lehetőleg mindig tartsanak maguknál egy kártyát, ami betegségükre felhívja az egészségügyi személyzet figyelmét. Súlyos esetben kórházba kell felvenni a beteget.
Az Addison-kórhoz gyakran társuló hipotireózisnak is fontos kezelési vonzatai vannak. Mivel az L-tiroxin-szubsztitúció a kortizol metabolizmusát gyorsítja, ez Addison-krízist provokálhat. Hipotireózis kórismézése esetén célszerű Addison-kór lehetőségére is gondolni, elsősorban a klinikai kép és a szérumelektrolitok figyelembevételével. Amennyiben e két betegség együttes fennállása valószínű, első lépésben mindig a hidrokortizon pótlásával kell kezdeni a kezelést.
Az Addison-kórban szenvedők kezelésének monitorozására az ACTH-plazmakoncentráció és a reninaktivitás mérését alkalmazzuk. Ezekkel az esetek többségében jól követhető a betegség lefolyása. A klinikai kép követése szintén fontos, mivel ez a laboratóriumi paraméterektől függetlenül is jelezheti a gyógyszeradagok módosításának szükségességét.
Levelezési cím: This e-mail address is being protected from spambots. You need JavaScript enabled to view it.
Ajánlott irodalom:
1. Igaz P, Rácz K, Tulassay Z. Autoimmun poliendokrin szindrómák és rokon kórképek: patogenezis és klinikai kép. Orv Hetil 2005;146:1531–1538
2. Gláz E. Addison-kór. In: Tulassay Z, szerk. A belgyógyászat alapjai. Medicina, Bp., 2011, 1520–1524
3. Rácz K. Addison-kór és izolált hypoaldosteronismus. In: Leövey A, Nagy VE, Paragh G, Rácz K, szerk. Az endokrin és anyagcsere-betegségek gyakorlati kézikönyve. Medicina, Bp., 2011, 316–328
a szerző cikkei
Nicole Michels, PhD
a szerző cikkei
Dr. Igaz Péter, kommentár
a szerző cikkei






