Szívelégtelenség gondozása beszédelemzéssel: a HearO applikáció
Mivel a szívelégtelenség a leggyakoribb halálozási ok, számos próbálkozás zajlik olyan noninvazív marker keresésére, ami a dekompenzációt időben jelzi előre. A CardioMEMS invazív módszere mellett immár létezik a telemedicina és a HearO applikáció noninvazív módszere is. Az itt használt biomarker a beszédanalízis. Nagyon-nagyon jól működik az algoritmus. Ezt mutatom be.
A beszédanalízis nem új megoldás, számos kereskedelmi vállalkozás használja szolgáltatásaihoz kényelmi és gyors megoldásként: ilyen az Amazon Alexája vagy az Apple Sirije, ugyanakkor a Google és a Netflix is kifejlesztette sajátját. De beszédanalízist használ az okoslakás is, például a fűtési rendszerében. Ennek visszásságára javaslom megnézni a következő vicces videót: a fogorvosi kezeléskor kapott érzéstelenítés okozta elkent beszéd milyen nehézséget okoz az okoslakás hangvezérlésében, https://www.youtube.com/ watch?v=nwPtcqcqz00. Az Amazon Halo Tone szolgáltatása okoskarkötőbe épített mikrofonokból épül fel. Ezek felveszik viselője hangját, az algoritmus pedig megállapítja, hogy az illető éppen boldognak, szomorúnak, izgatottnak vagy fáradtnak tűnik-e. Ezzel a karkötő viselői visszajelzést kaphatnak érzelmi állapotukról, ami segíthet nekik harmonikusabb kapcsolatokat fenntartani embertársaikkal. Az egészségügyben a beszédanalízist azonban eddig még alig használták.
A szívelégtelenség a kórházi felvételek egyik vezető oka, alapvetően a dekompenzáció kapcsán. A telemedicina lehetőséget nyújt arra, hogy a krónikus szívelégtelenségben szenvedő beteget dekompenzáció esetén időben ki lehessen emelni otthonából, ezzel elkerülhetővé téve a kórházi kezelést. Mivel a szívelégtelenség a leggyakoribb halálozási ok, számos próbálkozás zajlik olyan biomarker keresésére, ami időben előre jelzi a dekompenzációt. Évek óta létezik egy invazív módszer, ez a CardioMEMS HF System. Ez az arteria pulmonalis nyomásának mérésére való, az Egyesült Államok élelmiszer-és gyógyszerfelügyelete (FDA) által jóváhagyott implantált eszköz NYHA III. stádiumú szívelégtelenségben szenvedők esetén. Az a. pulmonalis nyomását mérve jelzi előre a pulmonalis pangást. A szenzor az éren belüli nyomásértékekről és a szívfrekvenciáról küld folyamatos tájékoztatást a hozzá vezeték nélkül csatlakozó monitorra és egy webfelületre, ahol a kezelőorvos követheti betege állapotát.
Úgy tűnik azonban, hogy formálódik egy noninvazív biomarker is, ez a telemedicina során alkalmazott beszédanalízis. Egy retrospektív vizsgálatban 10 583, telefonon történt és rögzített beteg–nővér beszélgetésből elemezték utólag a betegek beszédét. A rögzített telefonbeszélgetések egy krónikus betegekkel foglalkozó orvosi központ telemedicinás gondozásából származtak.1 A betegek közül 2267-en krónikus szívelégtelenségben, míg 8316-an más krónikus betegségben szenvedtek. A számos matematikai modellből, gépi tanulásból és informatikai megoldásokból felépített beszédanalízis felismerte azon jellemzőket (biomarkereket) a betegek beszédéből, melyek jelenléte 48%-kal növelte a későbbi szívelégtelenségből bekövetkező halálozási rizikót (95%-os megbízhatósági tartomány (MT): 1,39–1,58, p<0,001). Vagyis meg lehetett jósolni, ki lehet-e a beszédanalízissel azon, krónikus szívelégtelenségben szenvedő betegeket emelni, akik magas rizikójúak a dekompenzáció szempontjából.
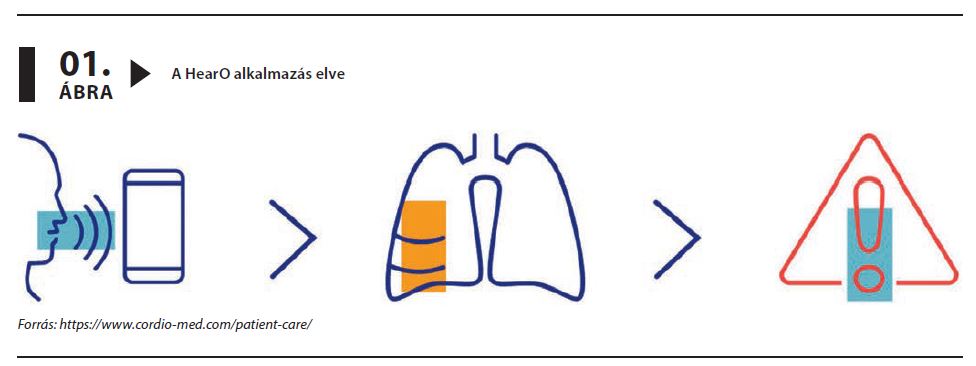 Egy másik vizsgálatban tervezett koronarográfiára készülő betegek beszédelemzése történt meg még a beavatkozás előtt (a betegek saját okostelefonjukra mondtak fel szöveget) (1. ábra). A szerzők találtak olyan szignálokat a beszédelemzés során, ami összefüggött a koronarográfiával igazolt coronaria-betegség jelenlétével.2
Egy másik vizsgálatban tervezett koronarográfiára készülő betegek beszédelemzése történt meg még a beavatkozás előtt (a betegek saját okostelefonjukra mondtak fel szöveget) (1. ábra). A szerzők találtak olyan szignálokat a beszédelemzés során, ami összefüggött a koronarográfiával igazolt coronaria-betegség jelenlétével.2
A már validálásra képes HearO alkalmazást használva végeztek egy egykarú, nyílt megfigyeléses vizsgálatot, amelyben beszédelemzést végeztek akutan dekompenzálódott szívelégtelenség kórházi kezelése előtt (a dekompenzált állapotban) és a kezelés után (kompenzált állapotban).3 A 40 résztvevővel lefolytatott vizsgálatban a betegek 5 mondatot ismételtek el (olvastak fel) 3-4 alkalommal. A hazaengedéskor végzett beszédanalízis 94%-ban tért el a dekompenzált állapotban végzetthez képest.
A HearO-t frappánsan tesztelték krónikus NYHA II–IV. stádiumú szívelégtelenségben szenvedő és hetente 2-3 alkalommal hemodializált betegeken is: a dialízis előtt és után, a dialízisek között több alkalommal.4 A dialízis előtti és utáni állapot jól modellezi a hidratáltságot. A szöveg felmondásának módszere a beszédanalízishez az előzővel teljesen ugyanaz volt. És itt is működött a beszédelemzés algoritmusával észlelt eltérés dialízis előtt és utáni elemzésben. Működik pulmonalis hypertonia esetén is,5 amikor a HearO algoritmusát katéterezés során nyert hemodinamikai adatokkal vetették össze 38 beteg esetén.
A fentiek direkt összefüggést nyilván nem igazolnak, de alapkísérletek bizonyították a patomehanizmust, és számos élettanilag feltételezhető mechanizmus létezik. Ilyen a nervus vagus szerepe, mert a X. agyideg részt vesz a hangképzésben (számos más agyideggel együtt), de a szív autonóm beidegzésében és a szívritmus kontrolljában is alapvető. A hidratáltság a hangszalagok rezgésében és a hangképző szervek működésében is meghatározó. A folyadéktúltöltöttség a fonációt azért befolyásolja, mert vizenyősek lehetnek a hangképző szervek is. Ez kihat például a hangok frekvenciájára is és a tüdőkben keltett rezgésekre (bronchophonia), melyek mind manifesztálódnak a hangképzésben a beszéd során.
 A HearO mobiltelefonon futó alkalmazás és rendszer (https://www.cordio-med. com) az app áruházakból nem letölthető, azonban a weboldalon elérhetőség szerepel, ami véleményem szerint azt jelzi, hogy az ellátóhely maga jelentkezhet be (mint a szívelégtelenségben szenvedő gondozottjai esetén a telemedicinát használni kívánó központ), és rajta keresztül lehet letölteni az általuk gondozott betegek számára a HearO alkalmazást. A HearO nem orvosi eszköz (medical device), vagyis nem az alkalmazás mond utasítást, terápiát, diagnózist a betegnek, hanem a telemedicina részeként alkalmazandó. Vagyis a rendszer végén szakember értékeli a látott adatokat és használja fel a telemedicinás vizit kapcsán ezt is a beteg állapotának megítélésére, majd dönti el azt, hogy valóban dekompenzálódik-e a beteg (2. ábra). A HearO tehát egy rizikószignál (noninvazív biomarker) a krónikus szívelégtelenség miatt gondozott beteg telemedicinás kontrollja során. Tehát ezért nem letölthető bárki számára, hanem az az orvosszakmai modell, hogy az intézmény regisztrál a rendszerért. Ezért érdemes szerintem intézményként felvenni a kapcsolatot a fejlesztő Cordio-Meddel. Az egyik vizsgálatban iPhone 6 Plus telefonon futott az app, az nem derül ki, hogy android verzió létezik-e.
A HearO mobiltelefonon futó alkalmazás és rendszer (https://www.cordio-med. com) az app áruházakból nem letölthető, azonban a weboldalon elérhetőség szerepel, ami véleményem szerint azt jelzi, hogy az ellátóhely maga jelentkezhet be (mint a szívelégtelenségben szenvedő gondozottjai esetén a telemedicinát használni kívánó központ), és rajta keresztül lehet letölteni az általuk gondozott betegek számára a HearO alkalmazást. A HearO nem orvosi eszköz (medical device), vagyis nem az alkalmazás mond utasítást, terápiát, diagnózist a betegnek, hanem a telemedicina részeként alkalmazandó. Vagyis a rendszer végén szakember értékeli a látott adatokat és használja fel a telemedicinás vizit kapcsán ezt is a beteg állapotának megítélésére, majd dönti el azt, hogy valóban dekompenzálódik-e a beteg (2. ábra). A HearO tehát egy rizikószignál (noninvazív biomarker) a krónikus szívelégtelenség miatt gondozott beteg telemedicinás kontrollja során. Tehát ezért nem letölthető bárki számára, hanem az az orvosszakmai modell, hogy az intézmény regisztrál a rendszerért. Ezért érdemes szerintem intézményként felvenni a kapcsolatot a fejlesztő Cordio-Meddel. Az egyik vizsgálatban iPhone 6 Plus telefonon futott az app, az nem derül ki, hogy android verzió létezik-e.
Az algoritmusok fejlődésével arra is lehetőség nyílik, hogy egyre nagyobb adathalmazokat felhasználva egyre pontosabb hang alapú biomarkereket társítsanak az egyes betegségekhez. Például a poszttraumás stressz szindrómában (PTSD) fejlesztettek egy gépi tanulással fejlődő programot a PTSD diagnosztizálására. Egy másik kutatásban egy hasonló analitikával működő algoritmus gyerekeknél támasztotta alá a depressziót és szorongásos tüneteket az elemzett hangminták alapján.
A Gartner technológiai elemző cég előrejelzése szerint 2022-re a mobileszközök 10%-ában már lesz beépített érzelemfelismerő mesterséges intelligencia, míg ez az arány 2018-ban még csak 1%-ot tett ki. Ha a HearO még több validálást igényel, és ha erre is keresnek centrumokat, akkor is érdemesnek tartom felvenni a kapcsolatot velük a megadott elérhetőségeken. Azt gondolom, nagyon ígéretes megoldást kínálnak a szívelégtelenségben szenvedő betegek gondozására.
Levelezési cím: This e-mail address is being protected from spambots. You need JavaScript enabled to view it.
A szerző munkahelye:
Dr. Speer Gábor: PhD, endokrinológus szakorvos. Biatorbágy Egészségügyi Központ / Egészségház – endokrinológiai ambulancia, Interlab Praxis Közösség és Plus Medical Orvosi Központ – endokrinológiai rendelések
Irodalom:
1. Maor E, et al. Vocal biomarker is associated with hospitalization and mality among heart failure patients. J Am Heart Assoc. 2020;9:e013359
2. Maor E, et al. Voice signal characteristics are independently associated with coronary artery disease. Mayo Clin Proc 2018;93:840–847
3. Offer A, et al. Remote speech analysis in the evaluation of hospitalized patients with acute decompensated heart failure. J Am Coll Cardiol HF 2021. December 8.
4. Amir O, et al. Feasibility of remote speech analysis in evaluation of dynamic fluid overload in heart failure patients undergoing haemodialysis treatment. ESC Heart Fail 2021;8:2467–2472
5. Sara JDS, et al. Non-invasive vocal biomarker is associated with pulmonary hypertension. PLoS One 2020;15:e0231441
a szerző cikkei