Lokálisan előrehaladott bazálsejtes karcinómás esetek parciális remissziója másodvonalban alkalmazott cemiplimabkezeléssel
BEVEZETÉS
A bazálsejtes karcinóma (BCC), más néven bazalióma világszerte a leggyakoribb rosszindulatú bőrtumor.1 Kialakulásában az ultraviola sugárzás kiemelendő mint fontos rizikótényező.2,3
A legtöbb bazalióma lokalizált és sebészeti úton eltávolítható, egyes esetekben alkalmazható sugárkezelés, illetve a szuperficiális típusú bazálsejtes karcinómára megoldást nyújthat számos helyi kezelés (krioterápia, imikimodkrém, fotodinámiás terápia (PDT) stb).4 A BCC-k egy része azonban multiplex megjelenésű, illetve lokálisan előrehaladottá válhat, igen kis hányaduk ritkán áttétet is képezhet, amely már irreszekábilis elváltozásnak minősül.5,6
Az előrehaladott, irreszekábilis BCC-ben szenvedő betegek kezelésében áttörést jelentett az SMO-inhibitor hedgehog szignál transzdukciós útvonalat blokkoló (hedgehoginhibitor, HHI) kezelés (vismodegib és sonidegib) megjelenése a terápiás palettán. Ezek a szerek elsődleges és másodlagos rezisztenciával járhatnak, illetve olyan toxicitási profillal rendelkeznek, amely megnehezíti a hosszú távú alkalmazásukat.6
2021 februárja előtt nem állt rendelkezésre előrehaladott bazálsejtes karcinóma esetén a HHI-kezelést követő, másodvonalbeli terápiás lehetőség.5 A pd-1-gátló cemiplimab-immunterápiát a közelmúltban (FDA 2021, EMA 2023) hagyták jóvá olyan előrehaladott BCC-ben szenvedő betegek számára, akik rezisztensek a hedgehoginhibitor terápiára, vagy nem tolerál- ják azt.6,7
ESETBEMUTATÁSOK

I. eset
64 éves férfi anamnézisében hipertónián kívül egyéb lényeges megbetegedés nem szerepelt. 2023-ban jelentkezett klinikánkon 10 éve nem gyógyuló, növekvő, kifekélyesedő elváltozása miatt. A klinikai kép a jobb vállon egy kb. 25 cm × 30 cm-es, mélyen exulcerált tumor volt (1. ábra). Szövettani vizsgálata mikronoduláris bazálsejtes karcinómát mutatott. Képalkotó vizsgálatok (teljestest-CT és regionális ultrahang) távoli áttétet nem jelzett.
Onkoteamünk 2023 szeptemberében, tekintettel az irreszekábilis, nagy kiterjedésű, mélyen ulcerált bazaliómára a jobb vállon, első vonalban vismodegibkezelést javasolt.
Egyedi méltányossági engedély birtokában betegünk 2023. november 8.–2024. február 7. között vismodegibkezelésben részesült (napi dózis: 1×150 mg). Mellékhatás a kezelés során nem jelentkezett, azonban a tumor javulást, regressziót nem mutatott, így onkoteamünk másodvonalban pd-1- gátló cemiplimab-immunterápia bevezetését javasolta.
2024 áprilisában elkezdtük a másodvonalbeli cemiplimabkezelést (háromhetente 350 mg dózisban, intravénás infúzióban), melyet a páciens jelenleg is kap. A terápia mellett a tumor regressziója megindult (2. ábra).
II. eset
88 éves férfi beteg anamnézisében multiplex bazalióma eltávolítás szerepel, illetve számos krónikus megbetegedés: Parkinson-kór, hipertónia, glaukóma, benignus prosztatahiperplázia, stroke (2024), pajzsmirigybetegség, köszvény.
2018-ban jelentkezett klinikánkon a homlokon lévő, korábban műtéti úton eltávolított bazalióma hegében kialakult recidív képlet miatt, melynek sebészi kimetszését javasoltuk, ezt azonban a páciens a teljes körű orvosi tájékoztatás ellenére sem vállalta.
2021 januárjában a megnövekedett tumorból (3. ábra) a beteg beleegyezésével szövettani mintavétel történt, mely infiltratív bazaliómát igazolt. Koponya-CT-vizsgálata a tumor okozta koponyacsont-destrukciót mutatott.
2021 februárjában onkoteamünk, tekintettel az inoperábilis, sugárterápiával sem kezelhető, lokálisan előrehaladott bazaliómára vismodegib kezelést javasolt, melyet egyedi méltányossági engedély birtokában 2021 áprilisától 2022 júniusáig, azaz 14 hónapig kapott.
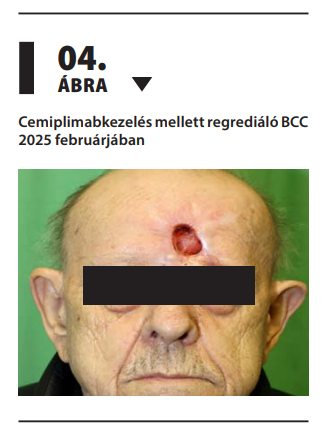
A vismodegibkezelést progresszió miatt leállítottuk, és másodvonalban cemiplimab PD-1-gátló immunterápia bevezetésére került sor, amely jelenleg is folyamatban van. A másodvonalbeli kezelés mellett a tumor regressziót mutat (4. ábra).
ÖSSZEFOGLALÁS
A daganatellenes kezelések az elmúlt évtizedben jelentős fejlődésen mentek keresztül. Előtérbe kerültek a célzott terápiák és az immunonkológiai szerek, háttérbe szorítva a hagyományos szisztémás kezelésként számontartott kemoterápiákat. Az immunterápiák indikációja egyre bővül, és egyre több daganatcsoportnál kerül sor a törzskönyvezésre, melynek eredményeképpen tartós tumormentesség érhető el.5
 Az immunellenőrzőpont-gátló (immune-checkpoint inhibitor) PD-1-gátló cemiplimab egy monoklonális antitest, amely a programozott sejthalál receptor- 1-hez (PD-1) kötődve gátolja annak interakcióját a PD-L1 és PD-L2 ligandumaival.6 A PD-1 receptor az aktivált immunsejtek, így a CD4, CD8, NK T-sejtek és a B-sejtek felszínén expresszálódik, csökkenti a T-sejt-aktivitást, ezáltal az immuntolerancia kialakításában és az autoimmunitás megelőzésében játszik szerepet. Ennek a gátlásnak a blokkolásával a PD-1-inhibitorok a T-sejtek aktivációjához járulnak hozzá. A gátlás alól felszabadult és aktivált T-limfociták hozzák létre a tumorellenes immunválaszt.6,8,9
Az immunellenőrzőpont-gátló (immune-checkpoint inhibitor) PD-1-gátló cemiplimab egy monoklonális antitest, amely a programozott sejthalál receptor- 1-hez (PD-1) kötődve gátolja annak interakcióját a PD-L1 és PD-L2 ligandumaival.6 A PD-1 receptor az aktivált immunsejtek, így a CD4, CD8, NK T-sejtek és a B-sejtek felszínén expresszálódik, csökkenti a T-sejt-aktivitást, ezáltal az immuntolerancia kialakításában és az autoimmunitás megelőzésében játszik szerepet. Ennek a gátlásnak a blokkolásával a PD-1-inhibitorok a T-sejtek aktivációjához járulnak hozzá. A gátlás alól felszabadult és aktivált T-limfociták hozzák létre a tumorellenes immunválaszt.6,8,9
A világ leggyakrabban előforduló daganata a bazálsejtes karcinóma, többnyire alacsony rizikójú tumor, könnyen kezelhető sebészi kimetszéssel, egy része sugárkezeléssel, illetve a szuperficiális bazalióma sok esetben nem sebészi módszerekkel is ellátható (krioterápia, PDT, helyi imikimodkrém, 5-fluorouracil kenőcs).4,5
A bazálsejtes karcinómák kis hányada azonban magas rizikójú daganatként jelenik meg, ezek azok az esetek, amelyeknél a recidívaarány magas, illetve azok a tumorok, melyek irreszekábilis, lokálisan előrehaladott daganattá válhatnak, illetve igen ritka esetben áttétet képezhetnek.2,10,11
Magas rizikójú bazálsejtes karcinómának számítanak azon bazaliómák, melyek 2 cm-nél nagyobb átmérőjű képletek a törzsön és a végtagokon; mérettől függetlenül azok a tumorok, amelyek a fejen, nyakon, lábfejen, tibia előtt és az anogenitális régióban helyezkednek el; a recidív tumorok; a perineurálisan terjedő daganatok; az agresszív szövettani típusok (infiltratív, mikronoduláris, morfeiform, bazoszkvamózus, szklerotizáló, karcinoszarkomatózus).11 Ugyanakkor az immunszuppresszív állapot, a sugárterápiával kezelt felületen jelentkező bazalióma és az immunellenőrzőpont-gátló kezelés mellett megjelenő bazálsejtes karcinómák is a magas rizikójú csoportba sorolandók.11
Az előrehaladott, irreszekábilis bazaliómák szisztémás kezelése első vonalban az SMO-inhibitor hedgehog szignál transzdukciós útvonalat blokkoló (HHI) kezelés (vismodegib, sonidegib), melyre az esetek nagy százalékában nagyfokú regresszió alakul ki (ORR 30–60%). Azonban rezisztencia kialakulásával számolni kell, illetve nem ritkán az életminőséget rontó mellékhatás is előfordulhat (ízérzés kiesése, kahexizálódás, simaizomgörcsök). Első vonalbeli HHI melletti progresszió esetén, illetve nem tolerálható mellékhatás előfordulásakor, másodvonalbeliként előrehaladott, irreszekábilis bazocelluláris karcinóma szisztémás kezeléseként PD-1-gátló cemiplimab adható.5,6
Az immunellenőrzőpont-gátló kezelések mellett szerteágazó, immunmediált mellékhatásokra számítani kell (leggyakrabban pneumonitisz, kolitisz, hipofizitisz, nefritisz, dermatitisz).5,6 Noha betegeinknél nem alakult ki adverz reakció, az immunterápia mellett a szoros követés, rendszeres laboratóriumi kontroll, belgyógyászati vizsgálat és képalkotóval való követés elengedhetetlen a kezelés során. A mellékhatások kezelése komplex gondolkodást kíván, és legtöbbször a társszakmák bevonását igényli.
Nyilatkozat. A közlemény más folyóiratban korábban nem jelent meg, és nem került beküldésre. A szerzők a cikk megírása, illetve a kutatómunka során anyagi támogatásban nem részesültek. A szerzőknek a cikk témájával kapcsolatos érdekeltsége nincs. A dolgozat nem sérti a Helsinki deklaráció előírásait.
Levelezési cím:
This e-mail address is being protected from spambots. You need JavaScript enabled to view it.
A szerzők munkahelye és beosztása:
Semmelweis Egyetem Bőr-, Nemikórtani és Bőronkológiai Klinika:
Dr. Kuzmanovszki Daniella: egyetemi adjunktus,
Dr. Tóth Veronika: egyetemi adjunktus,
Dr. Tóth Béla: egyetemi adjunktus,
Dr. Holló Péter: egyetemi tanár
Irodalom:
1. Guillaume T, Puzenat E, Popescu D, et al. Cemiplimab-rwlc in advanced cutaneous squamous cell carcinoma: real-world experience in a French dermatology department. Br J Dermatol 2021;185(5):1056-8
2. Puig S, Berrocal A. Management of high-risk and advanced basal cell carcinoma. Clin Transl Oncol 2015;17(7):497-503
3. Wu S, Han J, Li WQ, et al. Basal-cell carcinoma incidence and associated risk factors in U.S. women and men. Am J Epidemiol 2013;178(6):890-7
4. Goldenberg G, Hamid O. Nonsurgical treatment options for basal cell carcinoma - focus on advanced disease. J Drugs Dermatol 2013;12(12):1369-78
5. Stratigos AJ, Sekulic A, Peris K, et al. Cemiplimab in locally advanced basal cell carcinoma after hedgehog inhibitor therapy: an open-label, multi-centre, single-arm, phase 2 trial. Lancet Oncol 2021;22(6):848-57
6. Peris K, Fargnoli MC, Kaufmann R, et al. European consensus-based interdisciplinary guideline for diagnosis and treatment of basal cell carcinoma-update 2023. Eur J Cancer 2023;192:113254
7. Di Brizzi EV, Argenziano G, Brancaccio G, et al. The current clinical approach to difficult-to-treat basal cell carcinomas. Expert Rev Anticancer Ther 2023;23(1):43-56
8. Kuzmanovszki D, Kiss N, Toth B, et al. Real-World Experience with Cemiplimab Treatment for Advanced Cutaneous Squamous Cell Carcinoma-A Retrospective Single-Center Study. J Clin Med 2023;12(18)
9. Valentin J, Gerard E, Ferte T, et al. Real world safety outcomes using cemiplimab for cutaneous squamous cell carcinoma. J Geriatr Oncol 2021;12(7):1110-3
10. Eisemann N, Waldmann A, Geller AC, et al. Non-melanoma skin cancer incidence and impact of skin cancer screening on incidence. J Invest Dermatol 2014; 134(1):43-50
11. Heath MS, Bar A. Basal Cell Carcinoma. Dermatol Clin 2023;41(1):13-21
a szerző cikkei
Dr. Kuzmanovszki Daniella, Egyetemi adjunktus, Semmelweis Egyetem Bőr-, Nemikórtani és Bőronkológiai Klinika
a szerző cikkei







