A PRIME program újabb statisztikai adatai 2.
Az Európai Gyógyszerügynökség (EMA) PRIME programjának 3. szakaszába felvett, és az elutasított gyógyszereket ismertetjük.
Az első szakaszban, azaz április 6-ig a programba 18 jelentkezés érkezett, ezeket az EMA tudományos tanácsadói munkacsoportja (EMA’s Scientific Advice Working Party, SAWP), a fejlett terápiákkal foglalkozó bizottság (Committee for Advanced Therapies, CAT) és az emberi felhasználásra szánt gyógyszerek bizottsága (Committee for Medicinal Products for Human Use, CHMP) értékelte alkalmasságuk alapján. Erről korábbi cikkünkben számoltunk be.
A második szakasz jelentkezési határideje május 3. volt, a CHMP a befogadásról a június 20-23-i ülésén határozott. A CHMP 8 kérelmet bírált el. Ezek közül 2 befogadásra került, 6 kérelmet pedig a bizottság elutasított. Ezen felül 1 kérelem érkezett az EMA-hoz, amelynek értékelését a bizottság nem kezdte meg, mivel megítélése szerint kívül esett a program hatókörén. Lásd előző cikkünket.
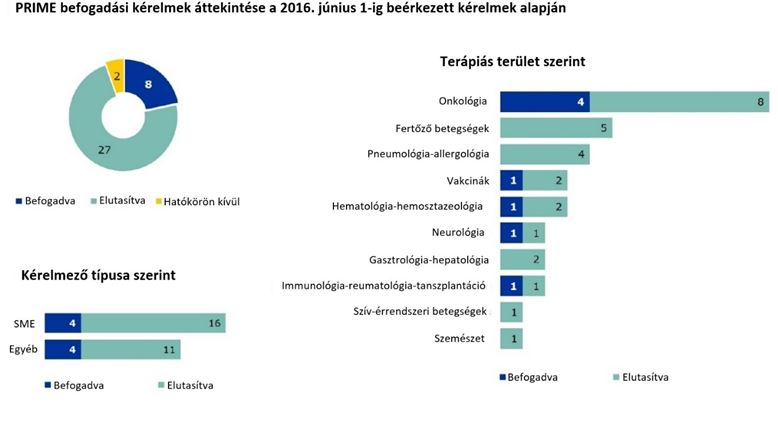
A harmadik szakaszban (jelentkezési határidő: 2016. június 1.) a július 18-21. ülésén határozott a CHMP. Összesen 9 kérelem érkezett, melyekből a bizottság 2 esetben döntött a befogadás mellett, 7 beadványt pedig elutasított. Ismét volt egy olyan kérelem is, amelyet a CHMP nem bírált el azzal a hivatkozással, hogy kívül esik a PRIME program hatókörén.
A kérelmek részletezése a jelentkezők típusa, a terápiás terület és a jelentkezést alátámasztó adatok típusa szerint:
|
PRIME: befogadott kérelmek (2 kérelem a beadott 9-ből) |
|||||
|
2016. július 27. (EMA/424593/2016) A PRIME programba történő befogadási kérelmek elbírálására vonatkozó ajánlások a CHMP 2016. július 18-21. ülésének határozata alapján a 2016. május 3-június 1. közötti időszakra. |
|||||
|
Név |
Hatóanyag típusa |
Terápiás terület |
Terápiás indikáció |
A kérelmet alátámasztó adatok típusa |
Kérelmező típusa |
|
Autológ CD4 és CD8 T-sejtek lentivirális vektorral bevitt megnövelt affinitású, a NY-ESO-1 (NY-ESO-1c259T) tumor antigént célzó T-sejt receptorral |
Fejlett terápia |
Onkológia |
Korábban kemoterápiában részesült, olyan inoperábilis vagy áttétes synoviális szarkómában szenvedő HLA-A*0201, HLA-A*0205 vagy HLA-A*0206 allélpozitív betegek kezelésére, akiknél a tumor az NY-ESO-1 tumorral rendelkezik |
Nemklinikai+ Klinikai kutatás |
SME |
|
Részleges E1A deléciót és egy integrinkötő domént (DNX-2401) tartalmazó 5-ös szerotípusú adenovírus |
Fejlett terápia |
Onkológia |
Olyan rekurrens glioblasztómában szenvedő betegek kezelésére, akiknél a teljes reszekció nem lehetséges vagy javasolható, illetve akik elutasítják a további sebészeti beavatkozást |
Nemklinikai+ Klinikai kutatás |
SME |
|
PRIME: elutasított kérelmek (7 kérelem a beadott 9-ből) |
||||
|
2016. július 27. (EMA/424593/2016) A PRIME programba történő befogadási kérelmek elbírálására vonatkozó ajánlások a CHMP 2016. július 18-21. ülésének határozata alapján a 2016. május 3-június 1. közötti időszakra. |
||||
|
Hatóanyag típusa |
Terápiás terület |
Terápiás indikáció |
A kérelmet alátámasztó adatok típusa |
Kérelmező típusa |
|
Biológiai |
Onkológia |
Relapszusos és refrakter myeloma multiplex kezelésére. |
Nemklinikai+ Klinikai kutatás |
Egyéb |
|
Biológiai |
Onkológia |
Gyermekkori diffúz hídi glióma (DIPG) kezelésére |
Nemklinikai+ Klinikai kutatás |
SME |
|
Biológiai |
Hematológia- Hemosztazeológia |
„A” típusú hemofília kezelésére |
Klinikai kutatás |
Egyéb |
|
Kémiai |
Hematológia- Hemosztazeológia |
Béta-thalasszémiában szenvedő betegek vastúladagolásának kezelésére |
Nemklinikai+ Klinikai kutatás |
SME |
|
Fejlett terápia |
Gasztroenterológia-hepatológia |
Aktív, középsúlyos-súlyos Crohn-betegségben (CD) szenvedő betegek kezelésére |
Nemklinikai+ Klinikai kutatás |
SME |
|
Kémiai |
Fertőző betegségek |
Invazív gombás fertőzések kezelésére |
Nemklinikai+ Klinikai kutatás |
SME |
|
Biológiai |
Pneumológia-allergológia |
Földimogyoró-allergia kezelésére |
Klinikai kutatás |
Egyéb |
Mi is az a PRIME?
Az Európai Gyógyszerügynökség (EMA) PRIME (PRIority MEdicines) programja olyan gyógyszerek számára válik elérhetővé, amelyek esetében főbb terápiás előny várható a már létező kezelésekhez képest, vagy olyan betegek számára lehetnek hasznosak, akiknél nem áll rendelkezésre kezelési lehetőség. A program nem pusztán az engedélyezést gyorsítja meg, hanem proaktívan nyújt támogatást: már a vizsgálatok megtervezése során tanácsokkal szolgál a gyógyszer előnyeire és kockázataira vonatkozó adatok begyűjtéséhez. Már a kísérletek és vizsgálatok megtervezése és beállítása során segíti, hogy jó minőségű adatok szülessenek, amelyek később megkönnyíthetik, meggyorsíthatják a forgalomba hozatali engedély értékelési eljárását, illetve lehetővé teszik a korlátozott erőforrások lehető legjobb kihasználását. Nagy gyógyszercégek számára is hasznos lehet, ám a program célcsoportja elsősorban a KKV (kis- és középvállalatok) és a tudományos (egyetemi, intézeti) szektor. A mikro-, kis- és középvállalatok (SME-k), valamint az akadémiai, felsőoktatási szektor szereplői ugyanis már figyelemre méltó nem-klinikai adatok és a kezdeti klinikai vizsgálatok tolerabilitási adatai alapján is pályázhatnak a programba. Ezen felül az SME-k és a tudományos intézmények kérvényezhetik a tudományos tanácsadási díjak alóli mentességet, valamint mivel jellemzően ezek a szereplők nem mozognak otthonosan az engedélyeztetési eljárások dzsungelében, különösen hasznos lehet számukra a PRIME-tól érkező iránymutatás.







