Új Janus-kináz gátló reumatoid artritisz kezelésére - frissítve
Az augusztusi amerikai engedélyeztetést követően az Európai Gyógyszerügynökség emberi felhasználásra szánt gyógyszerekkel foglalkozó bizottsága (CHMP) is pozitívan véleményezte a reumatoid artritisz kezelésére szolgáló Rinvoq (upadacitinib) készítményt.
- Új Janus-kináz gátló reumatoid artritisz kezelésére
- Biohasonló Humira
- Arthritisek elleni biohasonló szert engedélyezett az FDA (Eticovo)
- A Humira biohasonló gyógyszerét engedélyezte az FDA (adalimumab-adaz, Hyrimoz)
- AbbVie SAJTÓKÖZLEMÉNY
- Reumatológiai kórképek bizonyítékokon alapuló fizikoterápiája
- A 10 legjobbnak várt, késői fejlesztési fázisban lévő gyógyszer
Az Európai Gyógyszerügynökség emberi felhasználásra szánt gyógyszerekkel foglalkozó bizottsága (CHMP) október 17-én pozitív véleményt fogalmazott meg a reumatoid artritisz kezelésére szolgáló Rinvoq (hatóanyag: upadacitinib, gyógyszerforma: 15 mg-os retard tabletta, naponta egyszer) készítményre (kérelmező: AbbVie Deutschland GmbH & Co. KG). A teljes indikáció szerint a Rinvoq közepesen súlyos vagy súlyos aktív reumatoid artritiszben szenvedő olyan felnőtt betegek kezelésére javallott, akik elégtelen választ vagy intoleranciát mutattak egy vagy több betegségmódosító reumaellenes gyógyszerre (DMARD, disease-modifying anti-rheumatic drugs).
Az emberi felhasználásra szánt gyógyszerek bizottsága (CHMP) által az októberi ülésen adott pozitív vélemény a forgalmazási engedély kiadásának érdekében lefolytatott eljárás egyik legfontosabb állomása. A CHMP állásfoglalása most az Európai Bizottság elé kerül, és az intézmény dönt az uniós forgalomba hozatali engedély kiadásáról a CHMP pozitív véleményének kiadásától számított 67 napon belül. A termék alkalmazásával kapcsolatos részletes információkat az alkalmazási előirat (SmPC - Summary of Product Characteristics) tartalmazza majd, mely az Európai Unió összes hivatalos nyelvén elérhető lesz, amint az Európai Bizottság kiadja a forgalomba hozatali engedélyt. A forgalomba hozatali engedély kiadását követően az egyes uniós országok tagállami szinten döntenek majd a készítmény áráról és támogatásáról, figyelembe véve a gyógyszernek az adott ország nemzeti egészségügyi rendszerében betöltött várható szerepét, felhasználását.
Mellékhatások
A Rinvoq alkalmazása során tapasztalt leggyakoribb mellékhatások a felsőlégúti fertőzések, hányinger, megemelkedett kreatin-foszfokináz és köhögés voltak, a leggyakoribb súlyos mellékhatás pedig a súlyos fertőzés volt.
Tekintettel a reumatoid artritiszben szenvedő betegek ízületi fájdalmaira és csökkent kézügyességére, a Rinvoq dobozának kupakját úgy alakították ki, hogy még merev, fájdalmas ízületekkel is könnyen nyitható legyen, illetve a doboz szájának fóliáját is akadálymentesen lehessen kilyukasztani.
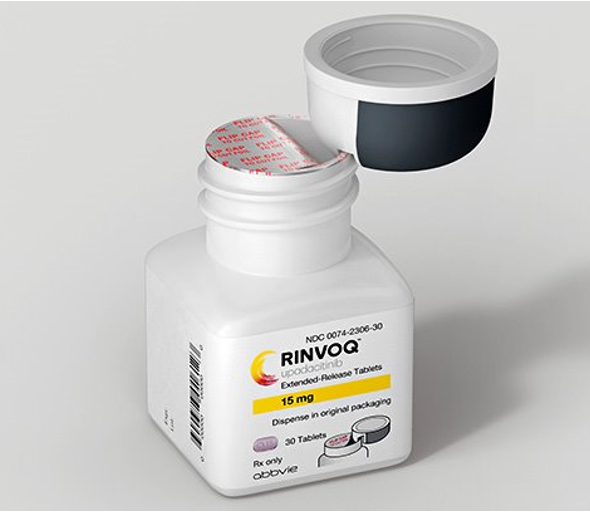
A Rinvoq dobozának különleges kialakítású kupakja, mely fájó ízületekkel is könnyen nyitható
A hatóanyagról (upadacitinib)
A Rinvoq hatóanyaga, az upadacitinib (ATC kód: L04AA44, korábbi vizsgálati kód: ABT-494) egy Janus-kináz (JAK) gátló, az AbbVie saját fejlesztése. A reumatoid artritisz (RA) patomechanizmusának ismert résztvevői az aktivált T-sejtek által stimulált B-sejtek és a monocita-makrofág rendszer sejtjei, amelyek jelentős mennyiségű gyulladásos citokint termelnek. A citokinek hatásukat a különböző sejteken megjelenő receptorok közvetítésével fejtik ki. Mivel e receptorok affinitása igen nagy, a citokinek már pikomoláris koncentrációban is hatásosak. Így a nyugvó sejteken kimutatható, sokszor csupán néhány száz receptormolekula is elegendő az intracelluláris jelsorozat megindításához és a biológiai hatás létrejöttéhez. A citokinek a célsejt membránreceptorához kapcsolódva aktiválják a receptort, ami ezután aktiválja a receptorhoz társult – egyes esetekben receptorkötött, más esetekben a citoszolból az aktivált receptorhoz kapcsolódó – foszforiláz enzimeket. Ezek újabb fehérjéket foszforilálnak, amelyek aktivált formában, legtöbbször dimerizálódva képessé válnak a sejtmagba jutni, ahol indukálják az adott citokinnek megfelelő DNS-szakaszon a megfelelő fehérje termelését. A legtöbb citokinreceptor a JAK-STAT (Signal Transducer and Activator of Transcription) jelátviteli úton fejti ki hatását.
A citokinreceptorok szerkezeti sajátságaik alapján különböző családokba sorolhatók, ezekre jellemző, hogy milyen foszforilázokat használnak. Az RA és számos gyulladásos mozgásszervi betegség kialakulásában és fenntartásában legfontosabb citokinek hatásai az I/II. típusú receptorokon keresztül érvényesülnek, ezek a vérképzésben, a limfoid és mieloid sejtek fejlődésében és számos, gyulladásban aktív szerepet játszó fehérje termelésében játszanak fontos szerepet, illetve az autoimmun gyulladás (például RA) fontos mediátorai. A JAK jellegzetessége, hogy a kinázdomén mellett tartalmaz egy pszeudokináz-domént is – éppen ezért nevezték el a kétarcú Janus római isten nyomán Janus-kináznak. A JAK-gátlók (jakinibek) a JAK enzimek foszforilációs aktivitását gátolják, mivel a foszforilációhoz használt ATP-kötődési helyükhöz kapcsolódva kompetitív módon megakadályozzák az ATP-kötést. Az első generációs jakinibek (tofacitinib, baricitinib, ruxolitinib, oclacitinib) többféle JAK-ot gátolnak (JAK1, JAK2, JAK3), különböző erősséggel, ami dózislimitáló mellékhatásokat eredményezett. Az upadacitinib újdonsága, hogy ez a hatóanyag már egy második generációs Janus-kináz gátló, ami a JAK1-re szelektív, így alkalmazása várhatóan kevesebb és jobban körülhatárolható mellékhatással jár.
Klinikai vizsgálatok
Az EMA a pozitív véleményt a fázis II BALANCE I és BALANCE II illetve CELEST vizsgálatokat követő SELECT program öt fázis III vizsgálatának eredményeire támaszkodva adta ki – ezekbe a klinikai vizsgálatokba összesen körülbelül 4400 beteget, többek között olyanokat is bevontak, akiknél kezelési kudarc vagy intolerancia lépett fel konvencionális, szintetikus betegségmódosító reumaellenes szerek (csDMARD, conventional synthetic disease-modifying antirheumatic drugs) alkalmazásakor, illetve akik nem mutattak megfelelő klinikai választ metotrexátra. A vizsgálatokban az upadacitinib az összes elsődleges és másodlagos végpontot teljesítette:
A SELECT-EARLY (NCT02706873) vizsgálatban a 12. héten az upadacitinibbel (Rinvoq, 15 mg/nap) monoterápiában kezelt metotrexát-naív betegek 52%-a ért el ACR50 választ, míg a metotrexáttal (szintén monoterápiában) kezelt betegeknél ugyanez 28% volt. A 12. hétre a Rinvoq-kal kezelt betegek 36%-a ért el klinikai remissziót (DAS28-CRP<2,6) a metotrexáttal kezelt betegek 14%-os arányával szemben.
A SELECT-MONOTHERAPY (NCT02706951) vizsgálatban a 14. héten a napi 15 mg Rinvoq-kal monoterápiában kezelt metotrexátra intoleráns vagy elégtelen választ mutató betegek 68%-a ért el ACR20 választ, ugyanez monoterápiás metotrexátkezelés esetében 41% volt. Az upadacitinibbel kezelt betegek 30%-a ért el klinikai remissziót (DAS28-CRP<2,6) a 14. hétre, szemben a placebo+metotrexát kar 8%-os arányával szemben.
A SELECT-COMPARE (NCT02629159) vizsgálatban a 12. hétre a napi 15 mg Rinvoq-kal és metotrexáttal kezelt metotrexátra intoleráns vagy elégtelen választ mutató betegek 71%-a ért el ACR20 választ a placebóval és metotrexáttal kezelt betegek 36%-os arányával szemben. A vizsgálatban részt vevő upadacitinibbel kezelt betegek 30%-a ért el klinikai remissziót (DAS28-CRP<2,6) a 12. hétre, szemben a placebo+metotrexát kar 6%-os arányával szemben.
A SELECT-NEXT (NCT02675426) vizsgálatban a napi 15 mg Rinvoq-kal és csDMARD készítménnyel kezelt, csDMARD készítmények monoterápiás alkalmazására intoleráns vagy elégtelen választ mutató betegek 64%-a ért el ACR20 választ, ugyanez a placebo plusz csDMARD kezelésben részesülő betegek esetében 36% volt.
A SELECT-BEYOND (NCT02706847) vizsgálatban a biológiai készítményekre intoleráns vagy elégtelen választ mutató betegek napi 15 mg-os Rinvoq plusz csDMARD kezelés hatására 65%-ban értek el ACR20 választ, míg placebo és csDMARD kezelés esetében ez az arány 28% volt.
A reumatoid artritiszről
Becslések szerint világszerte 23,7 millió, az Egyesült Államokban 1,3 millió, hazánkban körülbelül 50 ezer beteget érint ez a komplex, autoimmun eredetű betegség, melynek során az ízületeket bélelő hártyában kialakuló gyulladás következtében számos olyan anyag termelődik, amely a csontvégeket borító porcot és magát a csontot is károsítja. Az elsősorban a kéz- és lábkisízületeket, csuklókat, bokákat, térdeket, esetenként más ízületeket is szimmetrikusan érintő betegség a felszaporodó ízületi folyadékkal együtt jelentős fájdalmat, mozgáskorlátozottságot, deformálódást és következményes funkciókárosodást okoz, és a várható élettartamot 3-7 évvel rövidíti meg. A női-férfi arány 3:1, leggyakrabban 40-50 éves kor között jelentkezik. A betegségben megnő a fertőzésveszély, felgyorsul az érelmeszesedés, ezáltal növekszik a szív-érrendszeri halálozás, és valószínűleg megnövekszik a szekunder daganatok (főleg limfómák) rizikója is. A betegség eredetét nem ismerjük pontosan, több tényező egymásra hatása indítja el a folyamatot. Nem öröklődő betegség, de családi halmozódás előfordul; többféle gén felelős a genetikai fogékonyság és a betegség súlyosságának kialakulásáért. A már születéskor meglévő hajlam talaján környezeti és életmódi tényezők váltják ki a betegség létrejöttét, ilyen pl. a dohányzás, fogamzásgátlók szedése, stressz, bizonyos fertőzések.
Írásunk az alábbi közlemények alapján készült:
Summary of Opinion (SMOP)– Rinvoq (EMA)
FDA Approves AbbVie’s Rinvoq, a Potential Successor to Humira






